马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
本帖最后由 donglei 于 2017-4-7 10:13 编辑 + _- @( @' c: _ m, g' v" g+ E
' H& M% [+ J7 S! }1 ~% sClonal Evolutionary Analysis during HER2 Blockade in HER2-Positive Inflammatory Breast Cancer: A Phase II Open-Label Clinical Trial of Afatinib +/- Vinorelbine PLoS Med IF:13.585
, s* n6 r8 G- c6 m5 x; ]2 E, e文章概述
. Y/ q% {$ q i; F, C4 _2 Z7 K) E/ J1.II期开放式临床试验:HER2阳性炎性乳腺癌患者,阿法替尼单药 vs. 阿法替尼+长春瑞滨,单药治疗前后组织样本前瞻性全外测序;- d5 P4 |" ?. d. ~6 {% l% }2 b
2.阿法替尼单药治疗临床获益率35%,阿法替尼+长春瑞滨临床获益率20%,所有患者均存在治疗相关不良反应;
* t! w- `3 [2 J, A8 l3.与非炎性乳腺癌相比,炎性乳腺癌基因突变率升高(TP53),新抗原增加;9 J* y6 X1 s9 @0 i, d( f
4.治疗前后组织样本基因组变异结构具有一定稳定性,单药治疗前后克隆进化存在两种模式: branched evolution,shifting clonal structure
9 M( R1 x! S2 K2 l文章亮点
- I+ [' [. I9 C ]: W1.着眼于乳腺癌中恶性程度较高、已知信息较少的炎性乳腺癌(IBC)进行研究,一定程度上分析了非炎性乳腺癌(NIBC)与IBC之间的差异;2 b! i+ O8 k u1 S" X- d
2.EGFR、HER2双靶点抑制剂阿法替尼跨适应症应用探索;( r! y, u, Z$ {0 I$ Q7 o/ f: w
3.临床试验+基因组分析,结合临床信息从分子水平解析IBC特征;1 w: v& I0 C2 b! x
4.治疗前后节点取样,探究IBC阿法替尼单药治疗前后克隆进化过程
$ E# q2 H1 k& b/ I* L; Y/ h1.研究背景* Q9 `8 o8 G2 `$ p4 z3 ?8 |
1.IBC是一种发病年龄小、高侵袭性、不良预后、高转移性的乳腺癌亚型,总体发病率约占乳腺癌的1~6%;
8 e1 ?8 |% M* e3 c: D2.前期报道中,IBC突变频谱与NIBC相比有所不同,但整体景观仍未可知;
1 T Q% V; N# U$ l/ }5 d3.一些临床试验中,已有证据表明阿法替尼能使转移性乳腺癌患者获益(BIBW 2992,LUX-Breast 1)。. n) m. u8 ?& Q6 V
2. 试验设计+ |* D/ Z# N5 i, @
研究流程
: _. F9 }" j' M2 \# J$ [' W

4 ~ N3 k; X8 m+ g1.26名患者接受阿法替尼单药治疗(Part A);疾病进展后,10名患者接受阿法替尼+长春瑞滨联合治疗(Part B); X# W0 d: [ S
2.22名患者拥有治疗前组织样本,13名患者拥有治疗前后匹配组织样本. v# H- P$ z3 V
3. 试验结果分析- F. J+ R8 y: u P
患者临床获益比较7 M7 h+ Y5 {2 i
 % V7 Y: y3 K: w
% V7 Y: y3 K: w
1.单药治疗临床获益率35%,PFS中值110.5 days;26名患者中有7名接受过曲妥珠单抗治疗,在接受与未接受群体中阿法替尼临床获益率分别为0%(0/7)、47%(9/19),PFS中值分别为64 days、151 days& Z7 l, b3 y- L0 d
2.联合治疗临床获益率20%,PFS中值106.0 days;10名患者中有4名接受过曲妥珠单抗治疗,在接受与未接受群体中阿法替尼临床获益率分别为50%(2/4)、0%(0/6)* W O [! Z; x4 ?0 l, k5 l# _
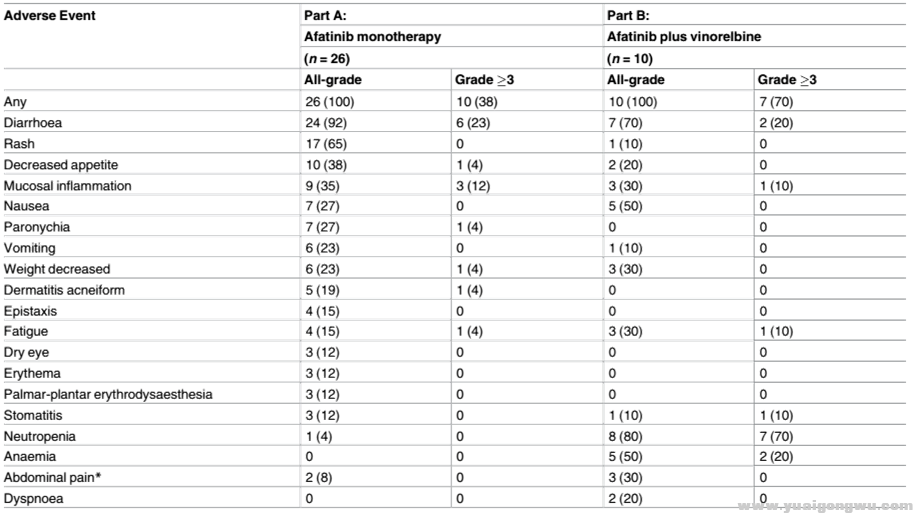
不良反应汇总+ Z( r m6 r2 k J
 7 o# q- z/ [, w; m
7 o# q- z/ [, w; m
1.无论是单药治疗还是联合治疗,不良反应率均达到100%
1 c; @( u1 H3 ~2 L2.3级以上不良反应率偏高(38%、70%)
- J- w$ {2 s' ~3 a' b3.单药治疗过程中,最常见不良反应及3级以上均为腹泻;联合治疗过程中,最常见不良反应为中性粒细胞减少及腹泻,最常见3级以上不良反应为中性粒细胞减少
; j# o* M8 F5 p4. HER2阳性IBC突变频谱分析1 Q4 a; ^' I8 X8 R: s f
22名患者疗前样本突变频谱分析# ]! k6 I `0 m& ^5 v# O; U

/ w. q) q8 [, x( s) r1.平均突变数:134.5(30–468),最常见突变基因为TP53(86.4% ,19/22)
% f0 o/ q+ w8 L R2.PI3K/AKT/mTOR通路相关基因突变率较高
2 ]* c" d" D$ O4 k+ o" F3.ERBB2扩增率并非100%,可能由于肿瘤异质性或正常组织污染造成1 R2 g. n2 N$ c$ I u4 W u* u
 ! M1 u3 i) X) q" Y' g9 A9 E
! M1 u3 i) X) q" Y' g9 A9 E
1.GISTIC分析确定了HER2阳性IBC患者染色体上4个常见扩增区域,及12个常见缺失区域9 m z1 z- ]$ ]2 Q/ \* ^9 Q
2.与NIBC相比,IBC非同义突变率上升,新抗原增加,TP53突变率上升
: G, g, P; z: v2 e9 r5. 治疗过程中的克隆进化分析
0 P: |% o& m& Z! O13对配对组织样本基因组分析
' A6 O, c) q; W" z7 g6 _0 ~
 / C$ p5 V _2 Z/ ~' h; r0 P* |
/ C$ p5 V _2 Z/ ~' h; r0 P* |
1.疗后13组织样本平均突变数181.4 (50–505),其中79.1% ± 12.0%突变与疗前配对样本共有" d8 \ n( m( H$ F6 }
2.治疗前后拷贝数变化也具有很强的一致性;分级群聚结果显示,肿瘤组织样本通过患者来源而并非治疗状态聚合- D, e9 @7 c' ?1 ? {$ G6 e7 o9 ]
两种克隆进化模式/ o! ]6 z; x |# h. u# q+ e' i
 7 G% Y# y# C# B: L" c e1 w: e! B
7 G% Y# y# C# B: L" c e1 w: e! B
T1:疗前节点样本 T2:疗后节点样本 CCF:cancer cell fraction Clonal cluster::T1、T2 CCF均接近1.0的肿瘤细胞克隆群(图中数字1代表,其余均为Subclonal cluster)
( J! `3 L3 I& s" {6 z8 ? L1.除主克隆外,亚克隆分别为两节点组织特有
3 S$ Y2 F' D2 b2.主克隆、亚克隆均为两节点组织共有,仅CCF在治疗过程中有升高或降低
$ F. M! j9 M4 r! R5 i) C6. 讨论
- J) N& ~3 V* s/ V1.阿法替尼单药或联合长春瑞滨均能使HER2阳性IBC患者获益6 M$ u9 F+ i* z8 y
2.HER2阳性IBC具有更高的突变及新抗原负荷,与NIBC相比,TP53突变率偏高是其显著的突变频谱特征- n; f+ y! B& t S) b
3.该研究中,治疗前后配对组织基因组分析没有发现突出的耐药性克隆,表观遗传学及微环境可能是IBC耐药性研究的未来方向
) P4 {5 T2 Z i转自吉因加科技微信订阅号, S5 ?3 _! {8 {
) f5 }+ t/ {0 ?) z, t |